第11話 プラスチックのはなし(2)[どんな格好なの・・]
皆さんはプラスチックを日常生活でよく目にしていると思います。
日用品や家電製品、そして、自動車等、様々な分野で使用されていますので、目で見る範囲ではプラスチックがどんなものかは、なんとなく判ると思います。
では、ミクロの世界ではどの様な格好をしているのでしょうか。
これから、プラスチック・・特にその中でも「熱可塑性樹脂」についてお話します。
プラスチックを小さく小さく見ると、実は多くは炭素原子と水素原子から成り立っています。
まず、高校の化学を思い出してくださいね。
炭素原子の記号(元素記号)は『C』ですね。そして、水素原子の記号(元素記号)は『H』です。
そして『C』の原子の質量(原子量)は12、『H』の原子の質量(原子量)は1です。
又、それぞれは他の原子と結びつくことができる腕を『C』は4本、『H』は1本持っています。
こんな具合です。
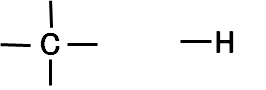
『C』と『H』で形づくられる最もシンプルな化合物は、『C』が1つで、4つの腕にそれぞれ『H』が結びついた「メタン」です。都市ガスはこれが主成分ですね。
次にシンプルなのは『C』が2つの「エタン」。その次が『C』が3つのプロパン。プロパンガスの主成分ですね。

ここから、プラスチックの元の化合物の話をします。
「エタン」の『H』と結びついている腕を、隣の『C』と両腕で結びつけたものが「エチレン」で、「プロパン」の『C』を両腕で結び付けたものは「プロピレン」と言います。なぜか「・・・レン」と呼びますね。
この「エチレン」「プロピレン」を人で例えると二人が両手をつなぎ合わせた形です。「プロピレン」は片方が少し頭でっかちの人のイメージですね。参考に「スチレン」も載せますが、「スチレン」は「プロピレン」の『CH3』のところに「ベンゼン環」という『C』が6個ついたもので、凄く頭でっかちな人が片方にいます。(図ではベンゼン環の『C』を省略して書いています)

それぞれの分子量は「エチレン」:28(『C』が2つで、『H』が4つですから・・)、「プロピレン」:42、「スチレン」:104です。
これらが、プラスチックの元になる化合物で、「モノマー」と呼びます。
では、これらがどうやってプラスチックになるかというと・・
それぞれのモノマーの両腕の片方を外して、隣のモノマーと腕をつなぐと、モノマー同士が連なることが出来ます。 この連ねてつなぐ操作を『重合』と言います。
限りなく長くつなげて、分子量が10,000程度以上になったものを「ポリマー(高分子)」と呼びます。 これがプラスチックです!!
【モノマー】 【ポリマー(高分子)】
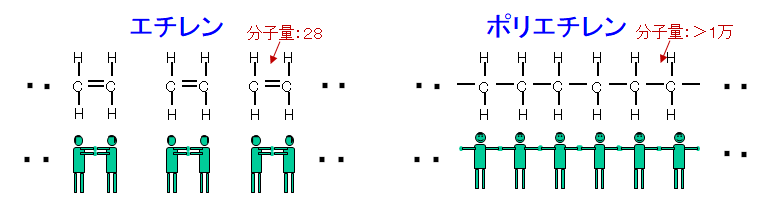
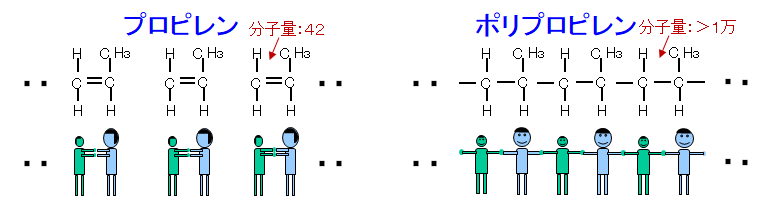
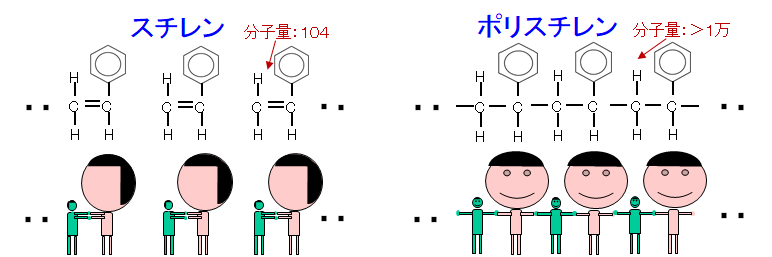
この様にプラスチックは「モノマー」が長く連なっていますので、まるで糸の様な格好をしているのです。
「エチレン」が糸の様に連なったものを「ポリエチレン」、「プロピレン」が連なったものを「ポリプロピレン」、そして、「スチレン」が連なったものを「ポリスチレン」と呼びます。
それぞれ、糸の様なものであるが故に、特徴的な性質を持ち、又、その糸を構成する「モノマー」によっても性質が異なります。
どの様に異なるか・・・については、その内、説明させていただきますね。


